ГОСТ 31114.3-2012 (IEC 61331-3:1998)
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
СРЕДСТВА ЗАЩИТЫ ОТ РЕНТГЕНОВСКОГО ИЗЛУЧЕНИЯ В МЕДИЦИНСКОЙ ДИАГНОСТИКЕ
Часть 3 Защитная одежда
Protective devices against diagnostic medical X-radiation. Part 3. Protective clothing and protectives for gonads
МКС 11.040.50
Дата введения 2015-01-01
Предисловие
Цели, основные принципы и порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием «Всероссийский научно-исследовательский институт стандартизации и сертификации в машиностроении» (ВНИИНМАШ)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 24 мая 2012 г. N 41)
За принятие стандарта проголосовали:
|
|
|
| Краткое наименование страны по МК (ИСО 3166) 004-97 |
Код страны по МК (ИСО 3166) 004-97 |
Сокращенное наименование национального органа по стандартизации |
| Азербайджан |
AZ |
Азстандарт |
| Беларусь |
BY |
Госстандарт Республики Беларусь |
| Казахстан |
KZ |
Госстандарт Республики Казахстан |
| Кыргызстан |
KG |
Кыргызстандарт |
| Российская Федерация |
RU |
Росстандарт |
| Таджикистан |
TJ |
Таджикстандарт |
| Узбекистан |
UZ |
Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 1 ноября 2012 г. N 660-ст межгосударственный стандарт ГОСТ 31114.3-2012 (IEC 61331-3:1998) введен в действие в качестве национального стандарта Российской Федерации с 1 января 2015 г.
5 Настоящий стандарт модифицирован по отношению к международному стандарту IEC 61331-3:1998* Protective devices against diagnostic medical X-radiation — Part 3: Protective glass plates (Средства защиты от рентгеновского излучения в медицинской диагностике. Часть 3. Защитная одежда) путем внесения дополнительных положений в 6.1, 7.1 и 8.3.
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. — Примечание изготовителя базы данных.
Степень соответствия — модифицированная (MOD).
Стандарт подготовлен на основе применения ГОСТ Р 51534-99 (МЭК 61331-3-98).
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта публикуется в ежемесячно издаваемом информационном указателе «Национальные стандарты».
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячно издаваемом информационном указателе «Национальные стандарты». В случае пересмотра или отмены настоящего стандарта соответствующая информация будет опубликована в ежемесячно издаваемом информационном указателе «Национальные стандарты»
Введение
Настоящий стандарт является прямым применением международного стандарта IEC 61331-3:1998 «Средства защиты от рентгеновского излучения в медицинской диагностике. Часть 3. Защитная одежда», подготовленного Подкомитетом 62 В «Аппараты для лучевой диагностики» Технического комитета МЭК 62 «Изделия медицинские электрические».
Настоящий стандарт не распространяется на защитные устройства, изготовленные из материалов, не содержащих свинец.
Для терминов, используемых в настоящем стандарте, применяют прописной шрифт.
1 Область применения и назначение
1.1 Область применения
Настоящий стандарт распространяется на защитные устройства, такие как ЗАЩИТНАЯ ОДЕЖДА, для защиты людей от ионизирующего излучения до 150 кВ во время медицинского рентгенологического исследования и лечения.
Примечание — Эти защитные устройства предназначены для использования с целью ослабления дозы облучения, когда другие методы защиты от ИОНИЗИРУЮЩЕГО ИЗЛУЧЕНИЯ не могут практически быть реализованы или недостаточны.
Требования настоящего стандарта являются обязательными.
1.2 Назначение
Настоящий стандарт устанавливает требования к:
— СОПРОВОДИТЕЛЬНЫМ (далее — ЭКСПЛУАТАЦИОННЫМ) документам, конструкции и используемым материалам;
— стандартным размерам, особенностям отдельных устройств, минимальным ОСЛАБЛЯЮЩИМ СВОЙСТВАМ материалов, маркировке и стандартизованным методам определения соответствия настоящему стандарту.
Стандарт рассматривает ЗАЩИТНУЮ ОДЕЖДУ, предназначенную для защиты ОПЕРАТОРА:
- — ЗАЩИТНЫЕ ФАРТУКИ;
- — ЗАЩИТНЫЕ ПЕРЧАТКИ;
- — ЗАЩИТНЫЕ РУКАВИЦЫ
и ЗАЩИТНЫЕ ПРИСПОСОБЛЕНИЯ для защиты пациента:
— ЗАЩИТНЫЕ ГОНАДНЫЕ ФАРТУКИ;
— ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД;
— ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ ЯИЧНИКОВ;
— ЗАЩИТНЫЕ ЭКРАНЫ.
Последняя группа ЗАЩИТНЫХ ПРИСПОСОБЛЕНИЙ предназначена для минимизации эффектов ОБЛУЧЕНИЯ во время РЕНТГЕНОЛОГИЧЕСКИХ исследований репродуктивных органов, в частности, для предотвращения генетических повреждений.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующий межгосударственный стандарт:
ГОСТ 31114.1-2002 (IEC 61331-1:1994) Средства защиты от рентгеновского излучения в медицинской диагностике. Часть 1. Определение ослабляющих свойств материалов.
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов по указателю «Национальные стандарты», составленному по состоянию на 1 января текущего года, и по соответствующим информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Определения
3.1 Терминология для определения степени требований
В настоящем стандарте использована следующая терминология:
«должен» — соответствие требованиям стандарта обязательно;
«рекомендуется» — соответствие требованиям стандарта рекомендовано, но необязательно;
«может» — используют для описания допустимых путей достижения соответствия требованиям стандарта;
«нормируемый» — используют для обозначения конкретной информации, содержащейся в ЭКСПЛУАТАЦИОННЫХ ДОКУМЕНТАХ, представленных ИЗГОТОВИТЕЛЕМ, или других документах, поставляемых с аппаратом и в основном касающихся его назначения, характеристик, условий эксплуатации и испытаний на соответствие.
3.2 Используемые термины
В настоящем стандарте применяют термины с соответствующими определениями по 3.3 и по IEC 60788 (приложение А) [1], которые в тексте выделены прописным шрифтом.
3.3 Определения терминов
3.3.1 ЗАЩИТНЫЙ ГОНАДНЫЙ ФАРТУК: Фартук, который надевает пациент для защиты области гонад вместо ПРИСПОСОБЛЕНИЙ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД или ПРИСПОСОБЛЕНИЙ ДЛЯ ЗАЩИТЫ ЯИЧНИКОВ (IEC 60788, МР-64-05) [1].
3.3.2 ЗАЩИТНЫЙ ЭКРАН: Экран для перекрытия ПУЧКА ИЗЛУЧЕНИЯ в области гонад, предназначенный для применения в том случае, когда ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД и ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ ЯИЧНИКОВ не могут быть использованы.
ЗАЩИТНЫЕ РУКАВИЦЫ: ЗАЩИТНЫЕ ПЕРЧАТКИ с открытой ладонью и отдельным большим пальцем, используемые тогда, когда необходима полная чувствительность при касании.
4 Общие положения
4.1 ЭКСПЛУАТАЦИОННЫЕ ДОКУМЕНТЫ
Защитные устройства должны быть снабжены ЭКСПЛУАТАЦИОННЫМИ ДОКУМЕНТАМИ.
ЭКСПЛУАТАЦИОННЫЕ ДОКУМЕНТЫ должны содержать:
— определение соответствия обозначения защитных устройств типу или индивидуальному обозначению;
— всю маркировку, нанесенную на устройство, и ее значение;
— ИНСТРУКЦИЮ ПО ЭКСПЛУАТАЦИИ, которая должна содержать:
а) правила хранения устройств,
б) рекомендованные методы и материалы для очистки и дезинфекции,
в) рекомендуемые методы и частоту периодических проверок пользователем, касающиеся ОСЛАБЛЯЮЩИХ СВОЙСТВ,
г) соответствие данному стандарту.
Если в ЭКСПЛУАТАЦИОННЫХ ДОКУМЕНТАХ инструкции содержат специальное руководство или информацию для ПАЦИЕНТА, должен быть приложен дубликат этих инструкций.
4.2 Язык ЭКСПЛУАТАЦИОННЫХ ДОКУМЕНТОВ
Данный стандарт не содержит требований к языку (языкам), на котором выпускают ЭКСПЛУАТАЦИОННЫЕ ДОКУМЕНТЫ.
Следует обратить внимание на то, что ЭКСПЛУАТАЦИОННЫЕ ДОКУМЕНТЫ, выпущенные на языке, отличном от того, на котором они были представлены и согласованы ИЗГОТОВИТЕЛЕМ защитных устройств, нуждаются в тщательной, по возможности, экспертной проверке, и должны иметь санкцию ИЗГОТОВИТЕЛЯ для использования в качестве таковых документов.
ЭКСПЛУАТАЦИОННЫЕ ДОКУМЕНТЫ должны содержать сведения о языке, на котором выпущен оригинал; в конце дается идентифицирующая ссылка на оригинальную версию.
4.3 Общие требования к маркировке
Защитные средства маркируют таким образом, чтобы была полная уверенность в их соответствии ЭКСПЛУАТАЦИОННЫМ ДОКУМЕНТАМ.
4.4 Конструкция
4.4.1 Защитные устройства для ОПЕРАТОРОВ должны быть изготовлены таким образом, чтобы их можно было надеть или снять без помощи ассистента (самостоятельно).
4.4.2 Защитные устройства для ПАЦИЕНТОВ должны быть сконструированы так, чтобы они были удобны в использовании и могли быть надеты и сняты самим ПАЦИЕНТОМ.
4.5 Материалы
4.5.1 Материалы, предназначенные для эффективного ОСЛАБЛЕНИЯ излучения, должны быть однородными и содержать элементы с высоким атомным номером.
4.5.2 ОСЛАБЛЯЮЩИЕ СВОЙСТВА не должны изменяться в условиях НОРМАЛЬНОГО ИСПОЛЬЗОВАНИЯ.
4.5.3 Все внешние и внутренние доступные средства защиты должны быть приспособлены для проведения их дезинфекции и должны быть моющимися, при этом указывают температуру моющих средств.
4.5.4 Должна быть исключена возможность касания с поверхностью, не имеющей покрытия, или с открытым металлическим свинцом, или его соединениями.
5 ЗАЩИТНЫЕ ФАРТУКИ
Примечание — ЗАЩИТНЫЕ ФАРТУКИ предназначены для использования персоналом, находящимся в процедурном помещении во время рентгеновского обследования, с применением и без применения процедур с внутренним вмешательством. Они предназначены в первую очередь для защиты основной части тела ОПЕРАТОРА. Чтобы защитить все тело, должны использоваться дополнительные средства, например для защиты щитовидной железы, очки или шлемы.
Приняты четыре категории ЗАЩИТНЫХ ФАРТУКОВ:
— легкие ЗАЩИТНЫЕ ФАРТУКИ;
— тяжелые ЗАЩИТНЫЕ ФАРТУКИ;
— легкие закрытые ЗАЩИТНЫЕ ФАРТУКИ;
— тяжелые закрытые ЗАЩИТНЫЕ ФАРТУКИ.
Примечание — Легкие ЗАЩИТНЫЕ ФАРТУКИ могут надеваться, например, в операционной зоне и в «гипсовом помещении» или в помещении, в котором обозначенная зона действия защищена от РАССЕЯННОГО ИЗЛУЧЕНИЯ другими средствами защиты, например средствами, зафиксированными на РЕНТГЕНОВСКОМ АППАРАТЕ.
5.1 Конструкция
ЗАЩИТНЫЕ ФАРТУКИ должны состоять из одного или более слоев защитного материала и должны закрывать переднюю часть тела от горла вниз до уровня коленей, покрывая полностью грудную клетку и плечи.
Ширина защитного материала на каждом плече должна быть не менее 11 см, и эти плечевые куски (полосы) должны закрывать заднюю часть плеч не менее чем на 15 см.
Незащищенные щелевые отверстия в месте фиксирования отдельных частей должны быть только на спине ЗАЩИТНОГО ФАРТУКА.
Примечание — РЕНТГЕНОВСКОЕ ИЗЛУЧЕНИЕ через щелевые отверстия в месте соединения частей может быть незначительным на спине из-за перемещений ОПЕРАТОРА относительно ИСТОЧНИКА РЕНТГЕНОВСКОГО ИЗЛУЧЕНИЯ.
Закрытые ЗАЩИТНЫЕ ФАРТУКИ должны закрывать дополнительно:
— боковые части тела от уровня не более 10 см ниже подмышек до не менее половины расстояния до бедра;
— спину до коленей.
Закрытые ЗАЩИТНЫЕ ФАРТУКИ должны быть устроены таким образом, чтобы была возможность воздушной вентиляции. Для этих целей можно предусмотреть перекрытия с креплением на боках, открытые части которых должны быть направлены к спине, или крепления, оставляющие вертикальную щель посредине спины.
Примечания
1 ЗАЩИТНЫЕ ФАРТУКИ могут состоять из двух перекрывающихся частей, жилета и юбки.
2 Допускается возможность добавления материала на ЗАЩИТНЫЕ ФАРТУКИ для увеличения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ в областях, где чувствительные органы могут подвергнуться опасности облучения во время отдельных исследований.
3 Закрытые ЗАЩИТНЫЕ ФАРТУКИ могут иметь перекрывающие друг друга крепления спереди.
5.2 Материалы
Защитные материалы, так же как фабричное покрытие и обшивка, должны быть гибкими.
а) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ легких ЗАЩИТНЫХ ФАРТУКОВ должен быть не менее 0,25 мм свинца на всей поверхности.
б) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ тяжелых защитных фартуков должен быть не менее 0,35 мм свинца на передней поверхности и не менее чем 0,25 мм свинца на остальных частях.
в) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ легких закрытых ЗАЩИТНЫХ ФАРТУКОВ должен быть не менее 0,25 мм свинца на всей поверхности.
г) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ тяжелых закрытых ЗАЩИТНЫХ ФАРТУКОВ должен быть не менее 0,35 мм свинца на передней поверхности и не менее 0,25 мм свинца для остальных частей.
5.3 Размеры
ЗАЩИТНЫЕ ФАРТУКИ классифицируют в соответствии с их стандартными размерами, приведенными в таблице 1.
Таблица 1 Стандартные размеры ЗАЩИТНЫХ ФАРТУКОВ
|
|
|
|
|
|
| Стандартный размер |
Буквенный символ |
Размер, см |
|
|
|
|
|
| Малый |
Очень короткий |
SV |
90 |
600 |
700 |
|
Короткий |
SS |
100 |
|
|
|
Средний |
SM |
110 |
|
|
|
Длинный |
SL |
120 |
|
|
|
Очень длинный |
SE |
130 |
|
|
| Средний |
Очень короткий |
MV |
90 |
600 |
850 |
|
Короткий |
MS |
100 |
|
|
|
Средний |
ММ |
110 |
|
|
|
Длинный |
ML |
120 |
|
|
|
Очень длинный |
ME |
130 |
|
|
| Большой |
Очень короткий |
LV |
90 |
750 |
1050 |
|
Короткий |
LS |
100 |
|
|
|
Средний |
LM |
110 |
|
|
|
Длинный |
LL |
120 |
|
|
|
Очень длинный |
LE |
130 |
|
|
| Примечания
1 Размер — длина от середины плеча до нижнего края.
2 Размер — ширина передней панели поверхности и задней панели ЗАЩИТНОГО ФАРТУКА, включая крепления (перекрытия) на боках.
3 Размер — ширина закрытого ЗАЩИТНОГО ФАРТУКА с креплением посредине спины.
4 Размеры , , являются минимальными размерами. |
5.4 Маркировка
Маркировка, нанесенная на ЗАЩИТНЫЙ ФАРТУК, должна быть ясной и постоянной, в виде лейбла (ярлыка), расположенного у края плечевой части фартука, и должна содержать следующую информацию:
а) наименование или торговую марку ИЗГОТОВИТЕЛЯ или поставщика (например xyz);
б) символ, соответствующий типу ЗАЩИТНОГО ФАРТУКА: L (легкий), Н (тяжелый), LC (легкий закрытый) или НС (тяжелый закрытый);
в) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ, выраженный символом Рb и числовым значением толщины свинца в миллиметрах.
Для всех ЗАЩИТНЫХ ФАРТУКОВ это значение относится к передней части, например: Рb 0,35 (спереди). Если есть отличия, приводят значение для задней части, например: Рb 0,25 (сзади);
г) АНОДНОЕ НАПРЯЖЕНИЕ для определения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ, следующее за маркировкой в соответствии с перечислением в) с добавлением косой черты, за которой следует значение АНОДНОГО НАПРЯЖЕНИЯ в киловольтах (/100).
ФИЛЬТРАЦИЯ, используемая для определения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ, зависит от АНОДНОГО НАПРЯЖЕНИЯ в соответствии с таблицей 3 ГОСТ 31114.1;
д) буквенные символы для размеров в соответствии с таблицей 1 (например LM);
е) ссылку на настоящий стандарт (ГОСТ 31114.3).
5.5 Определение соответствия
5.5.1 Соответствие ЗАЩИТНОГО ФАРТУКА требованиям настоящего стандарта формулируют следующим образом:
Тяжелый защитный фартук
xyz Н Pb 0,35/100 LM ГОСТ 31114.3-2012.
_______________
Наименование или торговая марка изготовителя или поставщика.
Символ ТЯЖЕЛОГО ЗАЩИТНОГО ФАРТУКА.
ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ.
АНОДНОЕ НАПРЯЖЕНИЕ (или ФИЛЬТРАЦИЯ).
Стандартный размер (большой, средний).
Ссылка на настоящий стандарт.
6 ЗАЩИТНЫЕ ПЕРЧАТКИ
Примечание — ЗАЩИТНЫЕ ПЕРЧАТКИ предназначены в первую очередь для применения медперсоналом во время рентгенологического исследования или лечения, в течение которого не исключается возможность того, что руки (кисти рук) и предплечья попадут в ПУЧОК ИЗЛУЧЕНИЯ или в область с высокой интенсивностью РАССЕЯННОГО ИЗЛУЧЕНИЯ.
6.1 Конструкция
ЗАЩИТНЫЕ ПЕРЧАТКИ должны закрывать руку полностью без промежутков и более половины предплечья. Должна обеспечиваться возможность промывания внутренней части перчатки.
ЗАЩИТНЫЕ ПЕРЧАТКИ должны быть устроены так, чтобы большой палец находился отдельно от остальных пальцев. Ось покрытия большого пальца должна быть повернута против ладони, чтобы обеспечивать возможность изгиба большого пальца к лицевой части при изгибе указательного пальца.
ЗАЩИТНЫЕ ПЕРЧАТКИ должны быть удобными для пальцев, закрытых ими; рука должна свободно сгибаться в запястье.
ЗАЩИТНЫЕ ПЕРЧАТКИ должны быть сделаны таким образом, чтобы в конечном счете требуемый минимальный ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ обеспечивался непрерывно по всей поверхности, лицевой и тыльной, включая пальцы и запястья.
ЗАЩИТНЫЕ ПЕРЧАТКИ должны изготовляться таким образом, чтобы какие-либо трещины и щели на используемом защитном материале, способные повлиять на уменьшение его ОСЛАБЛЯЮЩИХ СВОЙСТВ, могли быть обнаружены путем визуального осмотра. Любой материал покрытия должен быть отделяемым (любое покрытие должно быть съемным) для того, чтобы можно было осмотреть защитный материал при текущих проверках.
_______________
Только во вновь разрабатываемых конструкциях.
6.2 Материалы
Защитный материал и материалы покрытия для защитных перчаток должны быть гибкими.
Защитный материал ЗАЩИТНЫХ ПЕРЧАТОК должен иметь ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ не менее 0,25 мм по всей поверхности.
6.3 Размеры
ЗАЩИТНЫЕ ПЕРЧАТКИ должны соответствовать стандартизованным размерам, приведенным в таблице 2.
8.4 Маркировка
ЗАЩИТНЫЕ ГОНАДНЫЕ ФАРТУКИ должны иметь четкую и постоянную маркировку, содержащую следующую информацию:
а) наименование или торговую марку ИЗГОТОВИТЕЛЯ или поставщика (например xyz);
б) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ, выраженный символом Рb и числовым значением толщины свинца в миллиметрах (например Рb 0,5);
в) АНОДНОЕ НАПРЯЖЕНИЕ для определения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ, следующее за маркировкой в соответствии с перечислением б) с добавлением косой черты, за которой следует значение АНОДНОГО НАПРЯЖЕНИЯ в киловольтах (/100).
ФИЛЬТРАЦИЯ, используемая для определения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ, зависит от АНОДНОГО НАПРЯЖЕНИЯ в соответствии с таблицей 3 ГОСТ 31114.1;
г) буквенный символ, соответствующий размеру, указанному в таблице 2 (например А1);
д) ссылку на настоящий стандарт (ГОСТ 31114.3-2012).
8.5 Определение соответствия
Соответствие ЗАЩИТНОГО ГОНАДНОГО ФАРТУКА требованиям настоящего стандарта формулируют следующим образом:
Защитный гонадный фартук хуz Рb 0,5/100 А1 ГОСТ 31114.3-2012.
_______________
Наименование или торговая марка изготовителя или поставщика.
ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ.
АНОДНОЕ НАПРЯЖЕНИЕ (или ФИЛЬТРАЦИЯ).
Стандартный размер (взрослый 1).
Ссылка на настоящий стандарт.
9 ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД
Примечание — ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД, конструкция которых позволяет поместить в них мужские гонады, защищает гонады ПАЦИЕНТА от ненужного ОБЛУЧЕНИЯ ПУЧКОМ ИЗЛУЧЕНИЯ и от рассеянного излучения, облучения которым можно избежать, когда гонады находятся близко или в пределах надлежащим образом ограниченного ПУЧКА ИЗЛУЧЕНИЯ, например при РЕНТГЕНОЛОГИЧЕСКОМ исследовании таза.
Настоящий стандарт устанавливает две категории ПРИСПОСОБЛЕНИЙ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД:
— легкие ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД;
— тяжелые ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД.
В дополнение к требованиям согласно 4.1 ЭКСПЛУАТАЦИОННЫЕ ДОКУМЕНТЫ должны содержать рекомендации по применению доступных пластиковых пакетов, используемых вместе с ПРИСПОСОБЛЕНИЯМИ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД в гигиенических целях.
9.1 Конструкция
ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД должны закрывать мошонку или мошонку с пенисом полностью.
Приспособление должно быть устроено таким образом, чтобы ПАЦИЕНТ мог легко поместить его в нужное положение самостоятельно.
Открытая часть для ввода мошонки или мошонки с пенисом должна быть малой, насколько это возможно.
В ПРИСПОСОБЛЕНИЯХ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД должно быть предусмотрено сохранение их фиксированного положения во время РЕНТГЕНОЛОГИЧЕСКОГО исследования.
Приспособления должны быть изготовлены из защитных материалов с покрытием из водоотталкивающих материалов снаружи и внутри, позволяющих легко производить очистку и дезинфекцию.
9.2 Материалы
а) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ для легких ПРИСПОСОБЛЕНИЙ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД должен быть не менее 0,5 мм свинца по всей их поверхности;
б) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ тяжелых ПРИСПОСОБЛЕНИЙ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД должен быть не менее 1,0 мм свинца по всей их поверхности.
9.3 Размеры
ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД должны быть определенных размеров, иметь минимальный объем 80 см и максимальный объем приблизительно 300 см.
9.4 Маркировка
ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД должны иметь четкую и постоянную маркировку, содержащую следующую информацию:
а) наименование или торговую марку ИЗГОТОВИТЕЛЯ или поставщика (например xyz);
б) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ, выраженный символом Рb и числовым значением толщины свинца в миллиметрах (например Рb 1,0);
в) АНОДНОЕ НАПРЯЖЕНИЕ для определения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ, следующее за маркировкой в соответствии с перечислением б) с добавлением косой черты, за которой следует значение АНОДНОГО НАПРЯЖЕНИЯ в киловольтах (/100).
ФИЛЬТРАЦИЯ, используемая для определения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ, зависит от АНОДНОГО НАПРЯЖЕНИЯ в соответствии с таблицей 3 ГОСТ 31114.1;
г) ссылку на настоящий стандарт (ГОСТ 31114.3-2012).
9.5 Определение соответствия
Соответствие ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД требованиям настоящего стандарта формулируют следующим образом:
Тяжелое приспособление для защиты мужских гонад
xyz Pb 1,0/100 ГОСТ 31114.3-2012.
_______________
Наименование или торговая марка изготовителя или поставщика.
ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ.
АНОДНОЕ НАПРЯЖЕНИЕ (или ФИЛЬТРАЦИЯ).
Ссылка на настоящий стандарт.
10 ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ ЯИЧНИКОВ
Примечание — ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ ЯИЧНИКОВ, часто называемые «овариальные защиты», предназначены для защиты женских гонад ПАЦИЕНТОК от ненужного ОБЛУЧЕНИЯ ПУЧКОМ ИЗЛУЧЕНИЯ, когда яичники находятся в пределах надлежащим образом ограниченного ПУЧКА ИЗЛУЧЕНИЯ при передне-заднем просвечивании, например при РЕНТГЕНОЛОГИЧЕСКОМ исследовании в области таза.
10.1 Конструкция
ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ должны быть устроены таким образом, чтобы их можно было легко применять. Должна быть предусмотрена возможность сохранения положения защиты в течение всего РЕНТГЕНОЛОГИЧЕСКОГО исследования.
Приспособления должны быть изготовлены из защитных материалов с покрытием по всей поверхности водоотталкивающим материалом, позволяющим легко производить очистку и дезинфекцию.
10.2 Материалы
ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ ПРИСПОСОБЛЕНИЙ ДЛЯ ЗАЩИТЫ ЯИЧНИКОВ должен быть не менее 1,0 мм свинца по всей площади.
10.3 Размеры
За исключением случаев, когда применяют ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ ЯИЧНИКОВ специальной формы с возможностью регулирования размеров, они должны представлять собой набор разных форм и размеров.
10.4 Маркировка
ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ ЯИЧНИКОВ должны иметь четкую и постоянную маркировку, содержащую следующую информацию:
а) наименование или торговую марку ИЗГОТОВИТЕЛЯ или поставщика (например xyz);
б) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ, выраженный символом Рb и числовым значением толщины свинца в миллиметрах (например Рb 1,0);
в) АНОДНОЕ НАПРЯЖЕНИЕ для определения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ, следующее за маркировкой в соответствии с перечислением;
г) с добавлением косой черты, за которой следует значение АНОДНОГО НАПРЯЖЕНИЯ в киловольтах (/100).
ФИЛЬТРАЦИЯ, используемая для определения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ, зависит от АНОДНОГО НАПРЯЖЕНИЯ в соответствии с таблицей 3 ГОСТ 31114.1;
д) ссылку на настоящий стандарт (ГОСТ 31114.3-2012).
10.5 Определение соответствия
Соответствие ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ ЯИЧНИКОВ требованиям настоящего стандарта формулируют следующим образом:
Приспособление для защиты яичников
xyz Рb 1,0/100 ГОСТ 31114.3-2012.
_______________
Наименование или торговая марка изготовителя или поставщика.
ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ.
АНОДНОЕ НАПРЯЖЕНИЕ (или ФИЛЬТРАЦИЯ).
Ссылка на настоящий стандарт.
11 ЗАЩИТНЫЕ ЭКРАНЫ
ЗАЩИТНЫЕ ЭКРАНЫ, подвешиваемые над телом ПАЦИЕНТА, предназначены для перекрытия ПУЧКА ИЗЛУЧЕНИЯ в области гонад, их используют, когда не могут быть применены ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД И ЯИЧНИКОВ.
11.1 Конструкция
ЗАЩИТНЫЕ ЭКРАНЫ должны быть приспособлены для размещения между ИСТОЧНИКОМ ИЗЛУЧЕНИЯ и ПАЦИЕНТОМ таким образом, чтобы защищающие поверхности полностью закрывали область гонад.
ЗАЩИТНЫЕ ЭКРАНЫ должны быть приспособлены для применения со СВЕТОВЫМ УКАЗАТЕЛЕМ ПОЛЯ.
11.2 Материалы
ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ ЗАЩИТНЫХ ЭКРАНОВ должен быть не менее 1,0 мм свинца.
11.3 Размеры
За исключением случаев, когда ЗАЩИТНЫЕ ЭКРАНЫ изготовляют, чтобы иметь возможность некоторых изменений их формы и размеров, они должны изготовляться в виде набора нескольких подходящих форм и размеров.
11.4 Маркировка
ЗАЩИТНЫЕ ЭКРАНЫ должны иметь ясную и постоянную маркировку, содержащую следующую информацию:
а) наименование или торговую марку ИЗГОТОВИТЕЛЯ или поставщика (например xyz);
б) ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ, выраженный символом Рb и числовым значением толщины свинца в миллиметрах (например Рb 1,0);
в) АНОДНОЕ НАПРЯЖЕНИЕ для определения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ, следующее за маркировкой в соответствии с перечислением б) с добавлением косой черты, за которой следует значение АНОДНОГО НАПРЯЖЕНИЯ в киловольтах (/80).
ФИЛЬТРАЦИЯ, используемая для определения ЭКВИВАЛЕНТА ПО ОСЛАБЛЕНИЮ, зависит от АНОДНОГО НАПРЯЖЕНИЯ в соответствии с таблицей 3 ГОСТ 31114.1;
г) ссылку на настоящий стандарт (ГОСТ 31114.3-2012).
11.5 Определение соответствия
Соответствие ЗАЩИТНОГО ЭКРАНА требованиям настоящего стандарта формулируют следующим образом:
Защитный экран xyz Рb 1,0/80 ГОСТ 31114.3-2012.
_______________
Наименование или торговая марка изготовителя или поставщика.
ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ.
АНОДНОЕ НАПРЯЖЕНИЕ (или ФИЛЬТРАЦИЯ).
Ссылка на настоящий стандарт.
Приложение А
(обязательное)
Указатель терминов
В настоящем указателе для каждого термина указан соответствующий номер пункта раздела 3 «Определения» настоящего стандарта или обозначение термина по IЕС 60788 (МР-…) [1]. Знаком «+» и «-» отмечены производный термин без определения и термин без определения соответственно.
|
|
| АНОДНОЕ НАПРЯЖЕНИЕ |
МР-36-02 |
| ЗАЩИТНАЯ ОДЕЖДА |
МР-64-05+ |
| ЗАЩИТНОЕ ПРИСПОСОБЛЕНИЕ |
МР-64-05 |
| ЗАЩИТНЫЕ ПЕРЧАТКИ |
МР-64-05+ |
| ЗАЩИТНЫЕ РУКАВИЦЫ |
3.3.3 |
| ЗАЩИТНЫЙ ГОНАДНЫЙ ФАРТУК |
3.3.1 |
| ЗАЩИТНЫЙ ФАРТУК |
МР-64-05+ |
| ЗАЩИТНЫЙ ЭКРАН |
3.3.2 |
| ИЗГОТОВИТЕЛЬ |
МР-85-03- |
| ИЗЛУЧЕНИЕ |
МР-11-01 |
| ИНСТРУКЦИЯ ПО ЭКСПЛУАТАЦИИ |
МР-82-02 |
| ИСТОЧНИК ИЗЛУЧЕНИЯ |
МР-20-01 |
| КАБИНЕТ ЛУЧЕВОЙ ДИАГНОСТИКИ |
МР-20-22 |
| НОРМАЛЬНОЕ ИСПОЛЬЗОВАНИЕ |
МР-82-04 |
| нормируемый |
МР-74-02 |
| ОБЛУЧЕНИЕ |
МР-12-09 |
| ОПЕРАТОР |
МР-85-02 |
| ОСЛАБЛЕНИЕ (ОСЛАБЛЯЮЩИЕ СВОЙСТВА) |
МР-12-08 |
| ОСОБАЯ ЗОНА ПРЕБЫВАНИЯ |
МР-63-07 |
| ПАЦИЕНТ |
МР-63-03 |
| ПОВЕРХНОСТЬ ТЕЛА ПАЦИЕНТА |
МР-37-18 |
| ПОЛЬЗОВАТЕЛЬ |
МР-85-01 |
| ПРЕДЕЛ ЭКВИВАЛЕНТНЫЙ ДОЗЫ |
МР-61-01 |
| ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ МУЖСКИХ ГОНАД |
МР-64-06 |
| ПРИСПОСОБЛЕНИЯ ДЛЯ ЗАЩИТЫ ЯИЧНИКОВ (ЗАЩИТА ЯИЧНИКОВ) |
МР-64-07 |
| ПУЧОК ИЗЛУЧЕНИЯ (РАДИАЦИИ) |
МР-37-05 |
| РАССЕЯННОЕ ИЗЛУЧЕНИЕ |
МР-11-13 |
| РЕНТГЕНОВСКИЙ АППАРАТ |
МР 20-20 |
| РЕНТГЕНОЛОГИЧЕСКИЙ (РАДИОЛОГИЧЕСКИЙ) |
МР-40-02 |
| РЕНТГЕНОВСКОЕ ИЗЛУЧЕНИЕ |
МР-11-01 |
| СВЕТОВОЙ УКАЗАТЕЛЬ ПОЛЯ |
МР-37-31 |
| СОПРОВОДИТЕЛЬНЫЕ (ЭКСПЛУАТАЦИОННЫЕ) ДОКУМЕНТЫ |
МР-82-01 |
| ФИЛЬТРАЦИЯ |
МР-12-11 |
| ЭКВИВАЛЕНТ ПО ОСЛАБЛЕНИЮ |
МР-13-37 |
Приложение Б
(справочное)
Библиография
|
|
| [1] IЕС 60788:1984 |
Medical radiology — Terminology (Медицинская радиационная техника. Термины и определения) |
| ISO 3635:1981 |
Size designation of clothes — Definitions and body measurement procedure (Конструирование одежды по размерам. Процедура обозначения и измерения) |
| EN 340:1993 |
Protective clothing — General requirements (Защитная одежда. Общие требования) |
| EN 420:1994 |
General requirements for gloves (Общие требования к перчаткам) |

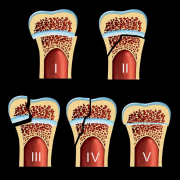
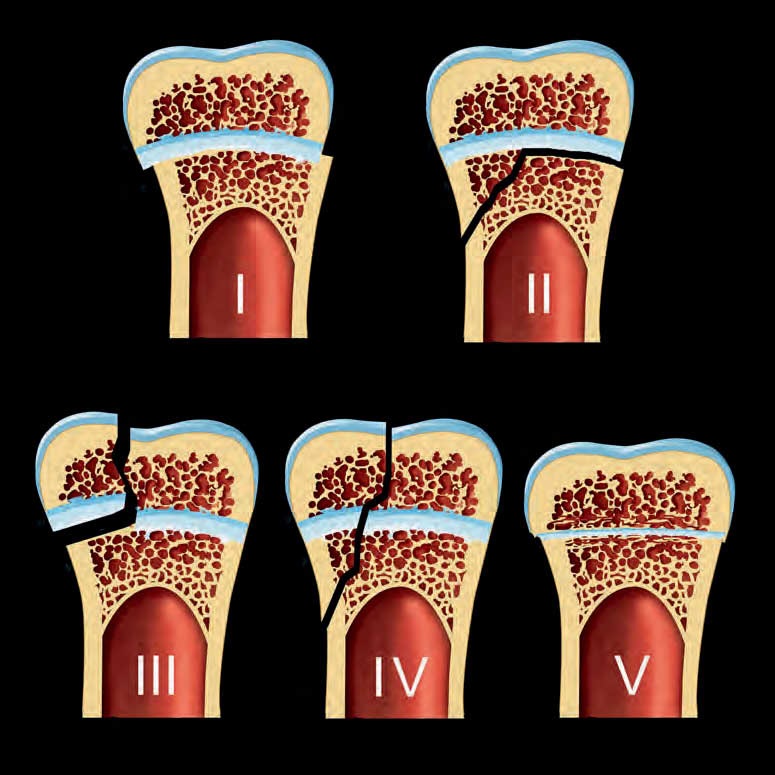
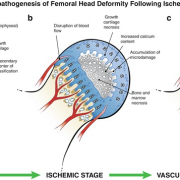
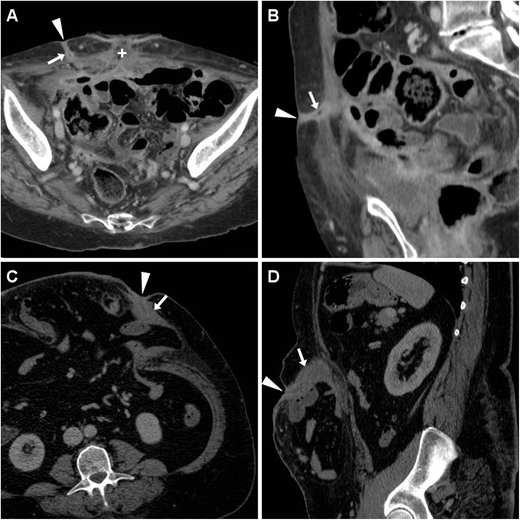
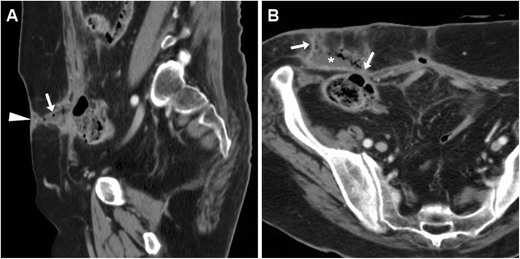
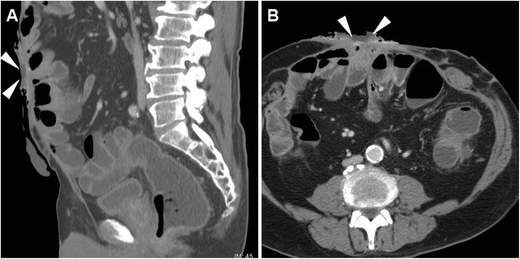
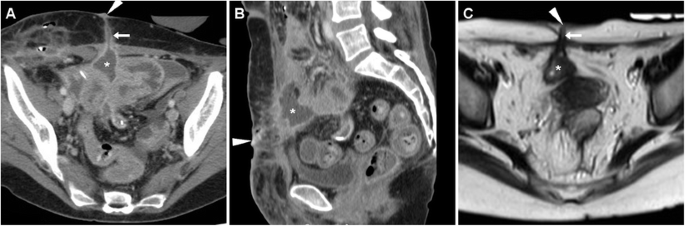
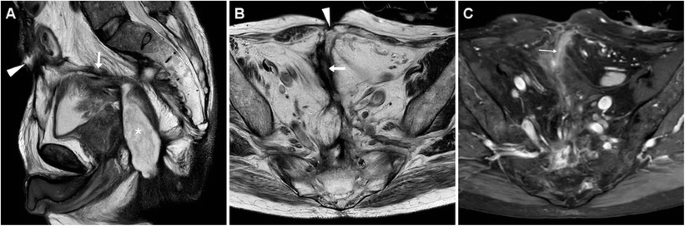
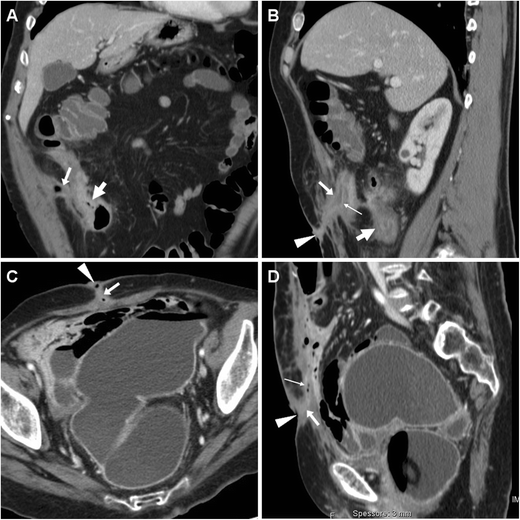
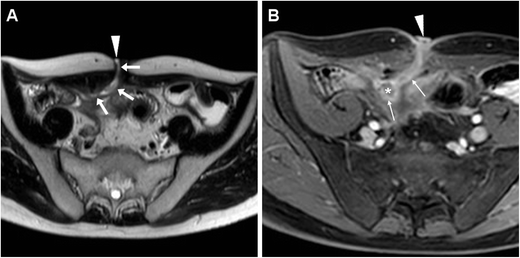
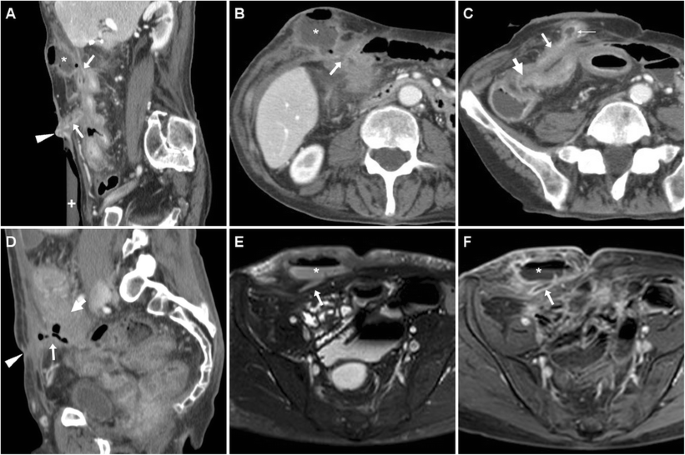
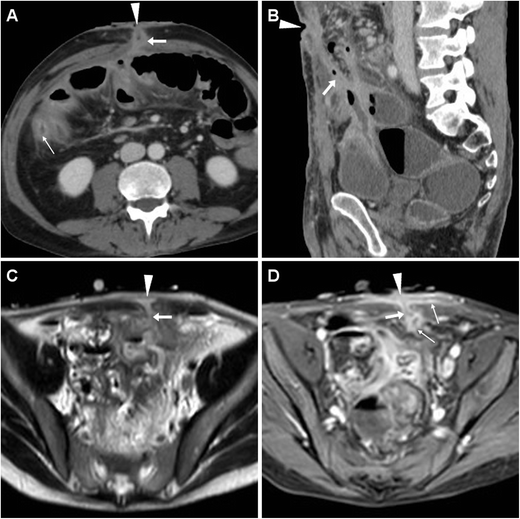

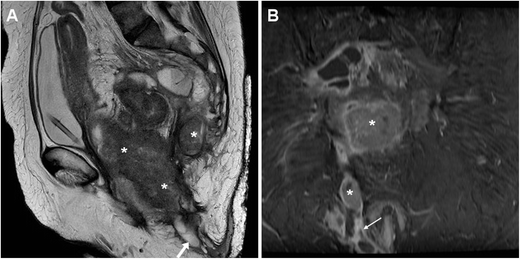
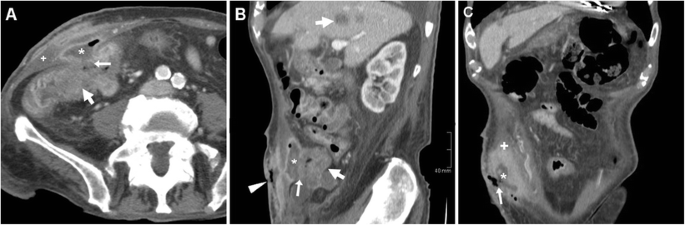



 Боснийская классификация, версия 2019 г., определяет кистозное образование почки как образование, которое, на основании субъективного визуального осмотра, состоит менее чем примерно из 25% усиливающих компонентов (
Боснийская классификация, версия 2019 г., определяет кистозное образование почки как образование, которое, на основании субъективного визуального осмотра, состоит менее чем примерно из 25% усиливающих компонентов ( 















































































 таблица доз радиации
таблица доз радиации